에이비온, 위암 신약 전임상 완료...글로벌 1상 추진 美 CRO 찰스리버와 'ABN401' 독성시험 마쳐, 한-호주 동시 임상
방글아 기자공개 2019-01-21 14:14:19
이 기사는 2019년 01월 21일 14:13 thebell 에 표출된 기사입니다.
에이비온이 위암 치료 신약의 전임상시험을 마치고 글로벌 임상에 나선다. 에이비온은 코넥스에 상장한 신약 개발 전문 업체로, 코스닥 상장사 케이피엠테크의 45.7% 자회사다.에이비온은 항암 치료 신약 'ABN401'의 전 임상시험을 완료했다고 21일 밝혔다. 지난 수 개월간 생물 소재 전임상시험 분야 세계 최대 CRO 기업 중 하나인 미국 찰스리버 랩(Charles River Laboratories)에서 독성시험을 진행했다.
에이비온의 핵심 신약 파이프라인인 ABN401은 간세포성장인자수용체(c-Met)가 변이된 암 환자의 치료 목적으로 투여하는 항암제 신약이다. 전세계 시장 규모가 15조원대로 평가되지만, 아직 시판 중인 특별한 치료제가 없는 실정이다.
에이비온은 전임상시험 결과를 토대로 글로벌 무대에서 본격적인 임상시험에 돌입할 계획이다. 에이비온 관계자는 "전임상시험 데이터를 포함한 임상시험 신청 준비 자료를 완성해1분기 내 제출할 예정"이라며 "호주에서 첫 해외 임상을 진행하고 동시에 국내에서도 임상 1상을 추진할 것"이라고 말했다.
에이비온에 따르면 회사는 앞서 미국 소재 의약품 제조 수탁기관(CMO)에서 임상 1상을 위한 경구용 제제 생산을 완료하고 시험성적서(COA)를 기다리고 있다. 에이비온 관계자는 "지난해 구조조정 등 도약을 위한 과정을 거친 만큼 올해부터는 신약 개발에 집중해 가속도가 붙을 것으로 기대한다"고 전했다.
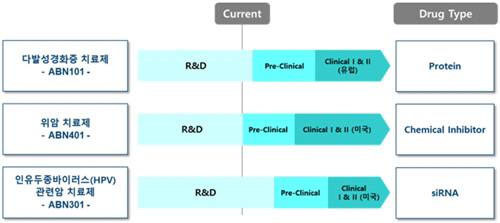
에이비온은 2007년 서울대학교 학내 기술벤처로 설립됐다. 현재는 ABN401 외 다수의 국가연구과제와 연계해 다발성경화증 치료용 단백질 치료제(ABN101), 인유두종바이러스(HPV) 관련암 치료제(ABN301)를 개발 중이다.
|
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- 수출입은행, 상반기 출자사업에 14곳 출사표
- 카카오, 2억달러 교환사채 발행 '공식화'
- [Red & Blue]수급 몰리는 피제이메탈, 알루미늄 시세 급등 '수혜'
- 이에이트, 가천대·길병원과 '디지털 트윈 병원' 구축 MOU
- [멀티플렉스 재무 점검]베트남만 남은 롯데시네마 해외사업
- [뮤지컬 제작사 열전]EMK컴퍼니, 고속성장 비결은 '대기업과 10년 동맹'
- 모트롤 인수 추진하는 두산그룹, 3년 전과 달라진 건
- [LG화학의 변신]패착된 NCC 증설, 자산 유동화 '제값 받기' 관건
- [캐시플로 모니터]포스코인터 '조단위 투자' 거뜬한 현금창출력
- [항공사 기단 2.0]'공격 확대' 에어프레미아·이스타, 매출·리스 줄다리기