코미팜, 긴급 임상신청 '코로나19' 치료제 작용기전은 파나픽스, 면역력 과다로 대규모 염증 반응 '사이토카인 폭풍' 억제…폐렴 증상 완화 기대
강인효 기자공개 2020-02-27 08:53:14
이 기사는 2020년 02월 27일 08:52 thebell 에 표출된 기사입니다.
신약 개발업체 코미팜이 자체 개발 중인 바이러스 감염증 치료제 후보물질인 '파나픽스'로 신종 코로나바이러스 감염증(코로나19) 치료제 개발에 뛰어들면서 해당 약물의 작용기전에도 관심이 쏠린다.코미팜은 26일 코로나19 환자 100명을 대상으로 파나픽스를 투여하는 임상 2상 및 3상을 진행하기 위한 긴급 임상시험계획(IND)을 식품의약품안전처에 신청했다고 밝혔다. 식약처로부터 IND 승인을 받을 경우 아시아태평양 전문 임상시험수탁기관(CRO) 노보텍(Novotech)이 코미팜과 코미팜호주법인(Komipharm International Australia Pty Ltd)의 지원을 받아 임상을 진행하게 된다.
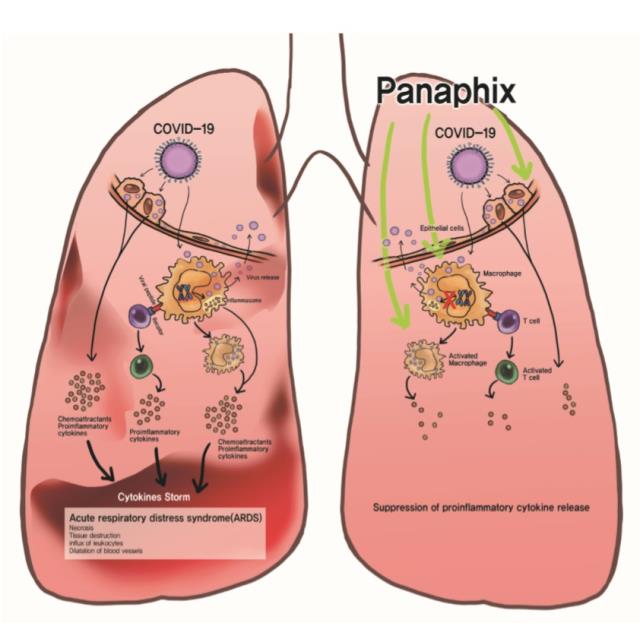
코미팜 관계자는 "코로나바이러스는 주로 코와 목에 접촉해 염증을 유발하는데, 현재 급격히 확산되고 있는 신종 코로나바이러스는 폐로 침투해 염증을 유발시킨다"며 "그러면서 공기가 있어야 할 폐포에 액체(고름)가 차게 해 호흡 곤란으로 일부 사망에 이르게 한다"고 설명했다.
이어 "신종 코로나바이러스가 인체에 침범하게 되면 체내 면역시스템이 작동해 외부의 적이 침범했다고 인지하고 과다한 염증성 면역세포가 폐로 보내진다"며 "과다하게 보내진 면역세포에서 배출된 사이토카인이 정상적인 폐 세포를 공격함으로써 다량의 염증을 발생시킨다"고 덧붙였다.
이처럼 외부에서 침투한 바이러스에 대항하기 위해 환자의 몸에서 과도하게 면역력이 증가해 대규모 염증 반응이 나오는 증상을 '사이토카인 폭풍(cytokine storm)'이라고 일컫는다. 사이토카인은 세포, 주로 백혈구에서 분비되는 단백질 면역조절제로서 특정 수용체와 결합해 면역 반응에 관여한다.
코미팜은 파나픽스가 사이토카인 폭풍을 억제함으로써 신종 코로나바이러스에 감염된 환자들의 폐렴 증상을 완화시킬 수 있을 것으로 기대하고 있다. 파나픽스는 면역세포의 신호전달 인자인 '인플라마솜(inflammasome)' 활성을 억제해 '염증 유발 사이토카인(염증성 사이토카인)'인 TNF-α, IL-1β, IL-6 등의 인자 배출을 막는다. 이러한 작용기전은 서울대 약대와 호주 퀸즐랜드대 연구 결과로도 확인됐다. TNF는 종양괴사인자(Tumor necrosis factor)를, IL은 인터루킨(Interleukin)을 말한다.
앞선 관계자는 "파나픽스 복용을 통해 체내 사이토카인 배출을 억제시키면 염증이 발생되지 않기 때문에 코로나19 초기 환자는 심각한 폐렴 증상을 겪지 않을 것"이라며 "중증이나 심각한 환자의 경우에도 폐렴 증상을 완화해 조기에 치료할 수 있을 것"이라고 밝혔다.
코미팜 관계자는 "전임상에 근거해 미국, 독일, 한국에서 폐렴 환자는 아니지만 372명의 사람(다른 질환 환자)을 대상으로 파나픽스 임상(1상)을 실시한 결과 안전성은 확보됐다고 믿고 있다"며 "이번 긴급 임상 신청으로 신종 코로나바이러스로 인한 폐렴 치료 효과 확인만이 남아 있는 단계"라고 밝혔다.
그러면서 "국내 및 제3국에서 신종 코로나바이러스 폐렴 환자를 대상으로 2주 정도 소요되는 긴급 임상을 실시한 뒤 결과를 보고고 환자에게 파나픽스를 공급할 계획을 갖고 있다"며 "파나픽스를 복용하면 코로나19 환자는 7일 정도면 병세가 호전되고, 14일 정도면 일상생활을 할 수 있을 정도가 될 것으로 예상하고 있다"고 덧붙였다.
2주간의 긴급 임상을 통해 효능이 확인되면 코로나19 환자에게 파나픽스의 처방이 가능하다는 의미다. 코미팜은 파나픽스의 임상 1상 결과를 토대로 코로나19 환자에게 가장 안전하고 효과를 극대화할 수 있는 복용량을 확정했다고 밝혔다.
파나픽스는 경구용 제제(먹는 약 형태)로, 코로나19 환자는 집이나 격리시설 등에서 편하게 복용할 수 있다는 장점이 있다. 아침 식사 직후 1정, 점심 식사 직후 1정, 저녁 식사 직후 1정 등 하루 총 3정을 복용하면 된다는 게 회사 측 설명이다.
코미팜은 충북 오송생명과학단지 내에 파나픽스 한 가지 제품만을 생산하는 우수 의약품 제조 및 품질 관리 기준(GMP) 인증 공장을 갖고 있다. 해당 공장의 현재 생산 가능 물량은 하루 30만정이지만 2배 정도 늘릴 수 있다.
회사 관계자는 "오송 공장 설비는 30만정을 매일 공급할 수 있는 생산 규모이며, 이는 10만명의 환자에게 매일 공급할 수 있는 물량"이라며 "파나픽스를 공급할 환자수가 증가할 경우 생산 인원을 증원하면 매일 60만정, 총 20만명의 환자에게 파나픽스를 공급할 수 있다"고 말했다.
코미팜은 임상약인 파나픽스의 생산에 대해서 미국 식품의약국(FDA)으로부터 제품 제조·품질 관리(CMC·Chemistry, Manufacturing and Control) 승인도 받았다. CMC는 임상용이나 상업용 의약품이 FDA가 정한 cGMP 규정에 맞게 제조됐는지 증명하는 자료다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- '3D 세포 관찰' 토모큐브의 상장 재도전, 예심 신청
- 'K-방산' MNC솔루션, 대표주관사 'KB증권'
- 율호,정부 핵심광물 공급망 확대 지원 선정
- 김연수 한컴 대표, '탁월한 선구안' AI 빅테크 이끈다
- CBI 관계사 지비이노베이션, 쌍전광산 장비설비 구축
- [간판펀드 열전]메가펀드 옛 영광 한투네비게이터 '리부트'
- 오가노이드사이언스, 기평 신청…사업성 입증 '관건'
- '개인안전장비 1위' 한컴라이프케어, 새 주인 찾는다
- [HD현대마린솔루션 IPO]고밸류 vs 저밸류…'피어그룹' 훌쩍 넘은 성장 여력
- [Company & IB]글로벌 신용평가 받은 롯데렌탈…'동향' 살피는 IB























