글로벌 퇴행성디스크 치료제 선두 경쟁 '지각변동' 메조블라스트 세포치료제 3상 재디자인…유한·엔솔바이오 'SB-01' 추격
최은수 기자공개 2022-05-17 14:11:03
이 기사는 2022년 05월 13일 09:59 thebell 에 표출된 기사입니다.
글로벌 퇴행성 디스크 치료제 시장의 경쟁 구도에 변화가 감지되고 있다. 가장 먼저 미국 FDA 임상 3상을 마친 메조블라스트(Mesoblast)의 줄기세포치료제 MPC-06-ID가 추가 임상을 진행하는 사이 경쟁사인 스파인바이오파마가 따라붙었다. 스파인바이오파마의 SB-01은 유한양행으로부터 기술을 이전받은 터라 국내 업계에서도 주목을 받는다.메조블라스트는 올해 1분기 FDA에 제출한 퇴행성 디스크치료제 후보물질 MPC-06-ID 3상 재설계 계획을 승인받았다. FDA 측에서 작년 말 관련 임상 3상 최종 결과를 검토한 뒤 약물 효과가 위약 대비 차이가 없거나 오히려 좋지 않았던 점을 지적한 데 따른 후속 조치다. MPC-06-ID는 중간엽줄기세포로 통증을 완화하는 기전이다.
메조블라스트가 임상 3상을 다시 진행하면 추적관찰 기간을 고려했을 때 2년 이상이 추가로 소요될 전망이다. 메조블라스트가 추가 임상의 1차 평가변수를 12개월 후 통증 감소 여부로 잡은 영향이다. 더불어 기존 임상 3상 참여 환자 중 20% 이상을 추가 임상에 포함시켜 치료 유효성과 통증 감소 여부를 입증할 계획이다.
업계 관계자는 "세포치료제의 경우 기전을 밝히는 것이 어렵고 환자마다 치료 반응이 다양하게 나타나 최근 미국이나 유럽에선 인·허가 사례가 줄어들고 있다"며 "더불어 기존 사용하는 약물도 금지하는 사례도 나타나고 있어 추가 임상을 진행한다 해도 상황을 낙관하기는 쉽지 않다"고 말했다.
메조블라스트가 임상 3상 막바지 단계에 다시 돌입한 가운데 직면한 사이 경쟁사 미국 스파인바이오파마도 올해 4월 SB-01의 임상 3상 IND를 승인받았다. 이에 따라 SB-01은 MPC-06-ID와 임상 진행 단계에서 어깨를 나란히 한 모습이다. 기존 SB-01와 MPC-06-ID와의 R&D 격차는 2년 이상 벌어져 있었다.
스파인바이오파마는 30곳의 의료기관에서 총 400명의 환자를 모집하며 올해 6월엔 임상 3상 첫 약물 투약에 나설 예정이다. 2024년 상반기엔 임상 결과를 확보할 것으로 전망된다.
스파인바이오파마는 국내 바이오벤처 엔솔바이오사이언스와 유한양행으로부터 기술을 이전받아 임상을 진행 중이다. SB-01은 P2K는 체내 TGF-β1에 작용해 신호전달 경로를 조절한다. 통증을 제어하고 디스크 퇴행 진행 방지 및 재생을 유도하는 기전이다.
엔솔바이오 관계자는 "SB-01은 퇴행성 디스크 치료제 퍼스트 인 클래스이자 연골 재생까지 기대할 수 있는 치료제로 개발 중"이라며 "계열 내 최초이자 근본 치료제 지위를 확보하고자 임상 상황과 경쟁 업체의 변화를 예의주시하고 있다"고 말했다.
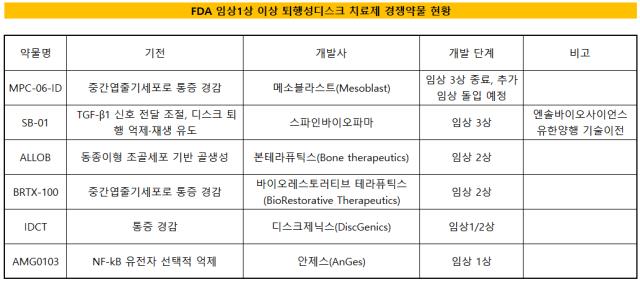
한편 전 세계 퇴행성 디스크 치료제 시장 규모는 2021년 말 기준 5조원에 달한다. 다만 아직 유효 치료제가 나오지 않아 환자들은 인공 디스크 삽입이나 통증 완화로 치료를 대체하고 있다. 현재까지 FDA 임상 1상 이상 R&D를 수행하는 업체는 전 세계 6곳이다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
best clicks
최신뉴스 in 전체기사
-
- [이통3사 AI 매치업]사물인터넷 회선 경쟁, AIoT 분야로 확전
- [컨콜 Q&A 리뷰]리스크관리와 주주환원책에 이슈 집중된 KB금융 IR
- KB금융, ELS 충격에도 견조한 이익창출력 과시
- [여전사경영분석]KB캐피탈, 우량자산 비중 확대 안정적 성장 관리 추진
- 수은, 첫 공급망기금채 발행…규모는 최대 3조
- [Policy Radar]보험사 감독강화 예고, 손보보다 부담 큰 생보
- 이복현 금감원장 "현안 대응 후 공직 마무리하겠다"
- [금융지주 해외은행 실적 점검]'동병상련' 농협·대구은행 미얀마 법인…회복 시동
- [캐피탈사 글로벌 모니터]하나캐피탈, 현지법인 손실 발생…사업 안정화 지원에 집중
- [저축은행 유동성 진단]KB저축, 예수금 축소에 유동성 개선 '제한적'
최은수 기자의 다른 기사 보기
-
- [클리니컬 리포트]박셀바이오, '가보지 않은' NK 췌장암 임상 '숨고르기'
- [제일약품의 온코닉테라퓨틱스 첫 '신약']'비상장 바이오벤처' 국산신약, 블록버스터에 도전장
- KDDF, 2기 체제 첫 인사 HLB제약 전복환 대표 영입
- 박셀바이오, 진행성 간세포암 타깃 'Vax-NK' 특허 출원
- 뷰노, '비파괴검사' 강자 이번엔 '안저분석' 혁신기기로
- [바이오텍 상장 재도전기]허리띠 졸라맨 벤처 10년, 건강한 비만약 실마리 찾다
- [클리니컬 리포트]티움바이오, TU2218 항암 적응증 '난치암'으로 확립
- 스카이테라퓨틱스, 심재학 엔솔바이오 CFO 영입
- [바이오텍 상장 재도전기]글라세움, 새 기전 '비만치료제' 인체서 반려견 '확장'
- [제약사 TSR 분석]보령, 뜻밖의 우주 주가향방 가른 '소통' 플러스 전환





















