브릿지바이오, BBT-301 L/I 선급금 15억 지급 완료 바이오벤처 셀라이온바이오메드에 전용실시권 확보+공동개발 "넥스트는 FDA IND"
최은수 기자공개 2023-10-24 11:14:41
이 기사는 2023년 10월 20일 10:32 thebell 에 표출된 기사입니다.
브릿지바이오테라퓨틱스가 셀라이온바이온메드로부터 기술이전(L/I) 받은 특발성 폐섬유증 치료제 BBT-301에 대한 계약 관련 선급금을 지급했다. BBT-301은 이온 채널이 일으키는 섬유화 질환을 타깃하는 특발성 폐섬유증 신약 후보물질이다.브릿지바이오테라퓨틱스와 셀라이온메드는 공동개발을 통해 이르면 반년 안에 미국 FDA 임상을 위한 IND(임상시험승인) 목적의 사전 미팅 진입을 목표로 한다. 해당 계약의 다음 마일스톤은 '미국 사업화 성과'로 확정한 셈이다.
◇옵션계약→전용실시권 확보 총 업프론트 '15억원' 지급 매조지
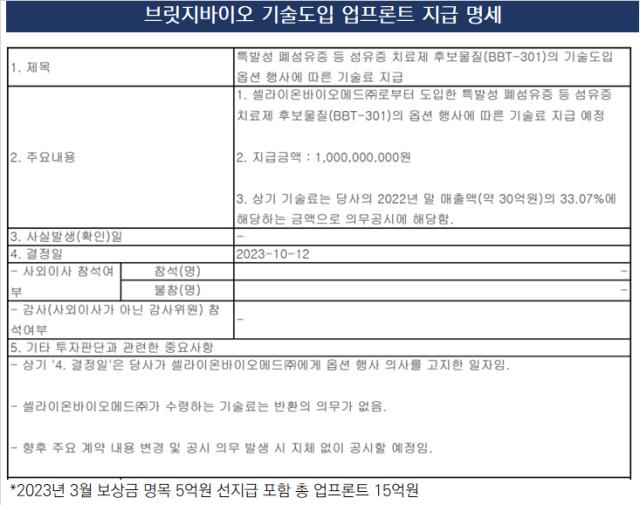
20일 업계에 따르면 브릿지바이오는 셀라이온바이오메드와 체결한 특발성 폐섬유증 치료제 후보물질 (개발명 BBT-301로 확정) 기술이전 계약과 관련 선급금을 지급했다. 브릿지바이오가 이번 지급했다고 밝힌 10억원인데, 작년 3월 양사가 처음 체결한 옵션딜에서 지급된 보상금 명목을 합치면 업프론트는 총 15억원이다.
BBT-301은 포타슘 채널(Kca 3.1)을 선택적으로 조절하는 기전의 특발성 폐섬유증 신약 후보물질이다. 기존 브릿지바이오가 개발 중인 파이프라인 BBT-877과 같은 적응증을 타깃한다. BBT-877은 역시 브릿지바이오의 핵심 자산 가운데 하나다. 최근 미국 식품의약국(FDA)으로부터 임상 2상을 승인받았다.
다만 BBT-877은 베링거인겔하임에 기술이전됐다가 독성 이슈로 반환을 받은 일례가 있다. 더불어 오토택신을 타깃한다. 포타슘 채널을 노리는 BBT-301과는 결이 다르다. 오토택신은 체내 지방 신호물질인 리소포스파티드산(LPA)을 생성하는 효소 단백질이다. 과도하게 형성되면 섬유화가 진행되는 부분에 착안해 BBT-877을 개발한다.
셀라이온바이오메드는 지난해 3월 특발성 폐섬유증 치료제 후보물질 BBT-301에 대한 전세계 전용실시권을 브릿지바이오에 양도하는 옵션 계약을 체결했다. 이후 양사는 비임상 약물 유효성 평가 등을 통해 기존 경쟁 약물 대비 우수한 효능과 안전성을 공동으로 탐색했다.
이어 지난 12일 브릿지바이오가 BBT-301의 효능과 안전성 검증을 마무리하면서 앞서 계약 가운데 전용실시권 옵션을 행사하면서 라이선싱 계약이 최종 확정됐다.
◇전 세계 난제 '섬유화' 넘을 실마리… 최대 시장 미국 조준
브릿지바이오는 셀라이온바이오메드와 함께 전 세계에서 개발에 난항을 겪는 섬유화증 치료를 위한 실마리를 BBT-301로부터 찾을 예정이다. 브릿지바이오가 글로벌 전용실시권을 도입하기 전인 지난해 8월 미국서 열린 특발성 폐섬유증 관련 국제 학회에서 해당 후보물질의 효능 및 효과 관련 주요 비임상 데이터를 공개한 것과 관련이 있다.
셀라이온바이오메드는 브릿지바이오와 협업을 이어가면서 개발 단계에 따른 중도 기술료 및 경상 로열티 등을 마일스톤으로 받게 된다. 더불어 브릿지바이오가 개발 중간 단계에서 제3자 대상 기술이전을 하는 경우 사전 합의된 비율대로 양사간 수익을 분배할 예정이다.
섬유화 질환은 간섬유화, 폐섬유화를 비롯한 심장, 신장 등의 여러 장기에 발생하는 치명적인 질환이며 유병률은 10만명 당 약 4900명으로 추정하고 있다. 특히, 특발성 폐섬유화 질환은 환자 수가 급격하게 늘어나는 질환으로 발병 후 생존율이 3~5년 밖에 안 되는 치명적인 질환이다.
현재로선 미국 사업화가 마일스톤 수령의 분기점이 될 예정이다. 이는 여러 글로벌 제약회사들도 오랜 기간 개발을 시도해 왔음에도 치료제 개발에 대한 미충족 수요가 매우 높은 것과 관련이 있다.
브릿지바이오는 이번 기술 도입 옵션 행사 이후 해당 후보물질의 신속한 글로벌 임상 진입을 위해 다음 사업화 순번을 미국 식품의약국(FDA)와의 임상시험 사전 미팅(Pre-IND meeting)으로 꼽았다. 최근 브릿지바이오의 자원이 BBT-877을 포함한 섬유화증 치료제 개발에 집중된 만큼 같은 적응증 파이프라인인 BBT-301도 선택과 집중 대상에 포함될 것으로 보인다.
셀라이온바이오메드 관계자는 "양사 협업으로 미국 임상 진입 등 성과를 창출하기 위해 노력할 것"이라며 "자금 조달도 계획 중이며 사업화를 진척하기 위한 기반을 다지는 시기"라고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- [한미 오너가 분쟁]임주현 "임종윤과 다른 길, 해외투자 유치는 곧 매각"
- [i-point]미래산업, 용인 반도체 클러스터 L-벨트 이전
- [한미 오너가 분쟁]소액주주 만난 임주현, 핵심은 'R&D' "한미정신 지킨다"
- '나형균호' 오하임앤컴퍼니, 사업 다각화 고삐
- [i-point]휴림로봇, 일반공모 유상증자 청약률 196.5% 기록
- [i-point]부스터즈, 네이버 스마트스토어·자사몰 매출 전략 강화
- '탄소제로 대비' 대우건설, 환경 에너지 정조준
- [시큐리티 컴퍼니 리포트] 시큐아이, 빅3급 실적에도 '보안 거리 먼' 임원들 우려
- [i-point]엑스페릭스-퓨리오사AI, UAE 방문 '협력 강화'
- 성장 돌파구 모색 KT스카이라이프, AI·아마스포츠 공략
최은수 기자의 다른 기사 보기
-
- 프레스티지바이오파마, 허셉틴시밀러 'EMA 승인권고'
- LG화학, '캐즘·석화불황' 보릿고개 넘는 비결 '바이오'
- [미지의 시장 '치매' 개화 길목에 서다]세번째 약물 '근본치료제'의 등장, 수십조 시장이 움직인다
- [Policy Radar]달라진 거래소 기조, 바이오텍 상장 심사 속도 빨라졌다
- [클리니컬 리포트]종근당, '10년의 도전' 탈모 '주사형' 차별화로 3상 진입
- 아보메드, 펀딩난에도 150억 시리즈C '멀티클로징' 막바지
- [제약바이오 시총분석]'잠재역량을 현실로' 유틸렉스, 잃었던 투심 회복 시작
- '100억 프리IPO' 레드엔비아, 상장 예심 청구 준비 '막바지'
- 아리바이오, 중국 기술이전 1200억 업프론트 확보 막바지
- [한미 오너가 분쟁]신동국-모녀 3자 주식매매계약, '한양정밀' 가세



















