대웅제약, 'DWJ1230' 2년만에 임상1상 재개한다 치료제 없는 과민성 장증후군 타깃…임상디자인 변경 후 환자 모집
최은수 기자공개 2023-01-06 13:59:13
이 기사는 2023년 01월 04일 15:16 thebell 에 표출된 기사입니다.
대웅제약이 2년 전 식품의약품안전처의 임상(1상) 승인을 받은 'DWJ1230'의 환자 모집을 재개했다.이 파이프라인은 국내에선 아직 뚜렷한 치료제가 개발되지 않은 설사 동반형 과민성 장증후군(IBS-D)을 타깃한다.
◇코로나19로 환자모집 난항→작년 말 변경 승인 후 재개
대웅제약은 기능성 설사 및 설사형 과민성 장증후군 증상을 보이는 대상자에게 DWJ1230을 반복투여한 후 혈중 중금속 농도를 평가하기 위한 임상 시험 환자 모집을 2일 공고했다.
해당 임상은 2021년 2월 첫 승인을 받았다. 다만 당시 코로나19 팬데믹 여파로 환자 모집을 임상 예상시기까지 마무리하지 못했다. 이에 작년 말 다시 임상변경승인을 받고 환자 모집을 재개했다.
해당 의약품은 국내개발을 목적으로 임상을 진행한다. 대상질환명은 △성인의 식도, 위·십이지장과 관련된 통증의 완화 △성인의 급·만성 설사 △24개월 이상 소아의 급성 설사 등이다.
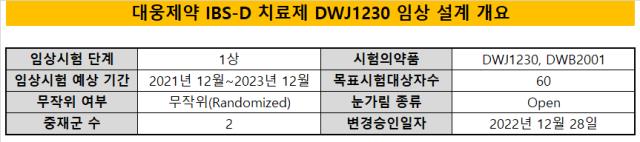
대웅제약은 세부적으로 임상시험을 공개, 무작위배정, 반복투여, 평행설계 형태로 꾸렸다. 국내에서 총 60명의 환자를 모집할 계획이다. 해당 임상에 대한 임상시험변경승인 시기는 작년 12월 28일이다. 장기간 환자가 모집되지 않으면서 시험계획을 일부 수정해 변경 승인을 받은 모습이다.
대웅제약은 DWJ1230 임상의 성공적인 수행 여부를 가늠하는 1차 평가변수를 임상시험용의약품 투여 후의 혈중 납 농도(Blood lead level)로 설정했다. 2차 평가변수는 투여 후의 납 외 다른 중금속(카드뮴, 비소, 수은) 농도, 임상시험용의약품 투여 후의 일정 수준의 중금속(코발트, 알루미늄) 농도다.
◇IBS-D 국내 치료제·처방 제한적…"연내 1상 종료 목표"
대웅제약이 DWJ1230을 통해 타깃하는 적응증은 과민성 장증후군(Irritable bowel syndrome, IBS) 중에서도 설사를 동반하는 질병(IBS-D)이다. IBS는 크게 변비를 동반하는 형태의 질환(IBS-C)과 설사형으로 나뉜다.
IBS-C와 달리 IBS-D의 경우 국내에 허가된 치료제가 많지 않다. 일본 제약사인 아스텔라스가 출시한 '이리보정'이 IBS-C가 남성 한정 치료제로 도입된 상태이며, 그 외에는 크게 꼽을 만한 치료제가 없는 상황이다. 유럽에서는 '트루버지(Truberzi)'를 비롯한 약물이 출시돼 시중에 유통중이다.
전 세계 IBS-D 시장 규모는 8억 달러(한화 1조원) 가량이다. 유럽 외에 미국에선 엘룩사돌린, 알로세트론, 리팍시민 등 약물을 제한된 형태로 투여하는 것이 권고된다. 세부적으로 엘룩사돌린은 담낭이 없거나 하루에 3잔 이상 음주하는 IBS-D 환자에겐 처방이 금지됐다. 리팍시민 또한 초기 반응 후 증상이 재발했을 때만 다시 치료하도록 권고한다.
이밖에 낮은 수준의 근거로 조건부 투여를 권고한 약물은 삼환계항우울제(TCA), 위장관 및 내장의 경련을 안정시키는 진경제 등이다. 국내에선 공식적인 치료제가 허가나지 않아 정확한 시장 규모가 집계되지 않는다. 현재로선 유산균(프로바이오틱스)을 비롯한 건강기능식품을 통해 IBS-D 증세 완화를 노리는 정도다.
대웅제약 관계자는 "국내에선 마땅한 치료 선택지가 없는 IBS-D에 대한 치료제로 개발을 시작했다"며 "1상 임상은 올해 말경 종료할 예정"이라고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- DS이앤이, 스마트 팩토리 첫발… 증축 공사 준공
- 쌍용정보통신, 1분기 매출 679억·영업손실 31억 기록
- [HLB '리보세라닙' 미국 진출기]진양곤 회장 "할 도리 다 했다, 남은 건 하늘의 뜻"
- [HLB '리보세라닙' 미국 진출기]아바스틴 왕위 잇는 '간암 타깃' 올인, '병용'으로 길 열었다
- 젬백스링크, 포니에이아이로부터 300억 투자유치
- [HLB '리보세라닙' 미국 진출기]K-바이오 모두가 주목한다, 미국 FDA 허가 결정 'D-1'
- [우리투자증권의 부활]'격전지' IB 비즈니스, 우리은행이 '열쇠' 쥐고 있다
- 드림텍, 반도체 모듈 사업 진출…인도서 모듈 양산
- 티에스넥스젠, 뉴로소나 투자로 글로벌 뇌질환 시장 진출
- [Red & Blue]엑스페릭스 품 떠나는 엑스플러스, 신사업 기대감 퍼질까
최은수 기자의 다른 기사 보기
-
- [HLB '리보세라닙' 미국 진출기]아바스틴 왕위 잇는 '간암 타깃' 올인, '병용'으로 길 열었다
- 유한양행, '넥스트 렉라자 찾아라' 기술교류 활발
- [이오플로우 '인슐렛' 소송 청신호]이오플로우, 골리앗과 미국 대결 우위…빅딜 불씨 되살린다
- 뉴라클사이언스, 상장·M&A 옵션 건 '프리 IPO' 유치
- [thebell note]바이오 '스타 애널리스트 CFO 시대'의 일몰
- 대웅제약, 편두통 보톡스 '플라시보' 부담에도 3상 간다
- [베일 벗은 통합 셀트리온]통합 후 첫 실적, 역대 최대 매출? 착시효과 해소는 '아직'
- 닥터노아, 뒤센근위축증 치료제 美 '희귀의약품' 지정
- '유한양행 포트폴리오' 바이오포아, 자금조달 초읽기
- 제넥신, 개발 전략 변경 '법률 비용 리스크'로 번졌다






















